Das Gesetz von Henry bringt zum Ausdruck, dass sich Gase unter Druck in Flüssigkeit lösen. Alle kohlensäurehaltigen Getränke sind von diesem Gesetz betroffen. Die Zufuhr von Kohlendioxid in Wasserflaschen erfolgt so z.B. unter hohem Druck. Öffnet man eine Wasserflasche erstmalig, ist der Druck in der Flasche höher als der Umgebungsdruck und die Kohlensäure entweicht. Dieses Phänomen nimmt mit der Zeit ab, bis sich ein Gleichgewicht einstellt. Beeinflußt wird dieser Vorgang durch Druck, Zeit und Temperatur.
Henry hat das Gesetz wie folgt formuliert:
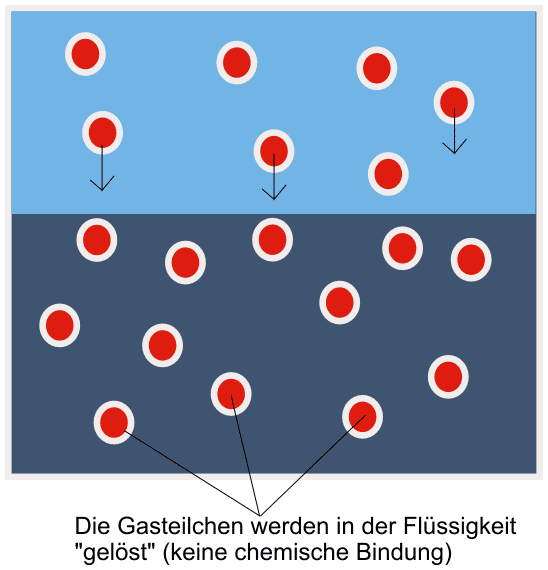
Bei konstanter Temperatur steht die Menge des in der Flüssigkeit gelösten Gases im Sättigungszustand in direktem Verhältnis zum Druck des über der Flüssigkeit stehenden Gases.
Für Taucher ist dieses Gesetz aufgrund des Verhältnisses von Sauerstoff und Stickstoff in unserer Atemluft von Bedeutung. Luft enthält zu 78% Stickstoff. Durch zunehmenden Druck beim Abtauchen löst sich immer mehr Stickstoff in unserem Blutkreislauf. Steigt ein Taucher zu schnell zur Wasseroberfläche auf, kann sich der Stickstoff nicht schnell genug aus dem Kreislauf lösen. Nach dem Gesetz von Boyle und Mariotte dehnt sich der Stickstoff aus und es entstehen Gasblasen.
Die Faustregel lautet:
Die Aufstiegsgeschwindigkeit von 10 Metern pro Minute sollte nicht überschritten werden. Zusätzlich sollte aus Sicherheitsgründen am Ende jeden Tauchgangs ein Sicherheitsstop auf 5 Metern für 3 Minuten eingehalten werden.
Da der Körper am Ende eines Tauchgangs in der Regel noch über eine Restsättigung an Stickstoff verfügt, muß diese Restsättigung bei einen eventuellen Folgetauchgang berücksichitgt werden.
